Simulado UNIRIO | Técnico de Laboratório – Química | CONCURSO
SIMULADO UNIRIO | TÉCNICO DE LABORATÓRIO – QUÍMICA
INSTRUÇÕES DESTE SIMULADO
OBJETIVOS DO SIMULADO
Aprimorar os conhecimentos adquiridos durante os seus estudos, de forma a avaliar a sua aprendizagem, utilizando para isso as metodologias e critérios idênticos aos maiores e melhores concursos públicos do País, através de simulado para concurso, prova de concurso e/ou questões de concurso.
PÚBLICO ALVO DO SIMULADO
Candidatos e Alunos que almejam sua aprovação no concurso UNIRIO para o cargo de Técnico de Laboratório – Química.
SOBRE AS QUESTÕES DO SIMULADO
Este simulado contém questões de concurso da banca CESGRANRIO para o concurso UNIRIO. Estas questões são especificamente para o cargo de Técnico de Laboratório – Química, contendo Química que foram extraídas de concursos públicos anteriores, portanto este simulado contém os gabaritos oficiais do concurso.
ESTATÍSTICA DO SIMULADO
O simulado UNIRIO | Técnico de Laboratório – Química contém um total de 20 questões de concursos com um tempo estimado de 60 minutos para sua realização. O assunto abordado é diversificado para que você possa realmente simular como esta seus conhecimento no concurso UNIRIO.
RANKING DO SIMULADO
Realize este simulado até o seu final e ao conclui-lo você verá as questões que errou e acertou, seus possíveis comentários e ainda poderá ver seu DESEMPENHO perante ao dos seus CONCORRENTES. Venha participar deste Ranking e saia na frente de todos. Veja sua nota e sua colocação no RANKING e saiba se esta preparado para conseguir sua aprovação.
Bons Estudos! Simulado para Concurso é aqui!
- #114533
- Banca
- CESGRANRIO
- Matéria
- Química
- Concurso
- UNIRIO
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 1 -
Uma massa de 0,0575 g de um sal foi medida em balança, foi dissolvida em água e transferida para um balão volumétrico, onde o volume final foi ajustado para 25,00 mL.
Considerando as devidas precisões dos aparatos e respeitando os algarismos significativos, a concentração, em g L -1 , da solução é
- a) 2
- b) 2,3
- c) 2,30
- d) 2,300
- e) 0.2 x 10 1
- #114534
- Banca
- CESGRANRIO
- Matéria
- Química
- Concurso
- UNIRIO
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 2 -
Considere os seguintes álcoois: metanol (CH3 OH), etanol (CH3 CH2 OH), propan -1 - ol (CH3 CH2 CH2 OH) e butan -1 - ol (CH3 CH2 CH2 CH2 OH).
Comparando-se algumas propriedades desses álcoois, verifica-se que o(a)
- a) metanol tem pressão de vapor menor do que a do propano - 1 - ol.
- b) butan - 1 - ol é mais solúvel em água do que o etanol.
- c) etanol, dissolvido em água, é menos ácido do que o propan - 1 - ol.
- d) massa específica do butan - 1 - ol é a menor dos álcoois da série apresentada.
- e) queima de 1 mol de butan - 1 - ol produz mais calor do que a queima de 1 mol de etanol.
- #114535
- Banca
- CESGRANRIO
- Matéria
- Química
- Concurso
- UNIRIO
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 3 -
A hidrazina se decompõe em gás nitrogênio e gás hidrogênio, segundo a equação abaixo
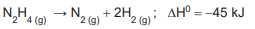
Em relação à sua vizinhança, ao decompor e formar produtos, esse sistema reacional
- a) perde calor e perde energia na forma de trabalho.
- b) perde calor e ganha energia na forma de trabalho.
- c) ganha calor e não realiza trabalho.
- d) ganha calor e perde energia na forma de trabalho.
- e) ganha calor e ganha energia na forma de trabalho.
- #114536
- Banca
- CESGRANRIO
- Matéria
- Química
- Concurso
- UNIRIO
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 4 -
A decomposição da água é representada na reação termoquímica abaixo.

A variação de entalpia, em kJ, de formação de 1 mol de H2 O(g) será de
- a) +286
- b) -286
- c) +572
- d) -572
- e) +1144
- #114537
- Banca
- CESGRANRIO
- Matéria
- Química
- Concurso
- UNIRIO
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 5 -
O teor de mercúrio em um padrão certificado de água é 1,46 mg L-1 . Uma análise, com três réplicas, foi realizada, e os resultados obtidos, em mg L-1 , foram: 1,50, 1,52 e 1,54.
Sendo assim, o erro relativo da análise, em %, e o maior desvio obtido, em mg L-1 , são, respectivamente:
- a) 1,0 e 0,10
- b) 3,2 e 0,04
- c) 3,2 e 0,08
- d) 4,1 e 0,04
- e) 4,1 e 0,08
- #114538
- Banca
- CESGRANRIO
- Matéria
- Química
- Concurso
- UNIRIO
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 6 -
Um técnico possui quatro tipos de placas de metal (de cobre, de zinco, de chumbo e de prata) e soluções aquosas de sulfato de cobre, de sulfato de zinco, de nitrato de chumbo e de nitrato de prata.
Uma reação química redox espontânea ocorre quando a placa de

- a) zinco é colocada na solução de sulfato de zinco.
- b) prata é colocada na solução de nitrato de cobre.
- c) cobre é colocada na solução de sulfato de chumbo.
- d) chumbo é colocada na solução de nitrato de prata.
- e) chumbo é colocada na solução de nitrato de zinco.
- #114539
- Banca
- CESGRANRIO
- Matéria
- Química
- Concurso
- UNIRIO
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 7 -
O tipo de risco, ao qual um indivíduo estará exposto ao manusear um produto químico, é indicado no pictograma usado nas rotulagens. A partir dos pictogramas, o usuário é alertado para os cuidados que devem ser tomados, a fim de se evitarem acidentes. Considere que, no rótulo de um frasco, onde há uma determinada substância química, está o pictograma representado a seguir.

Esse pictograma indica que a substância é
- a) tóxica
- b) oxidante
- c) inflamável
- d) corrosiva
- e) gás sob pressão
- #114540
- Banca
- CESGRANRIO
- Matéria
- Química
- Concurso
- UNIRIO
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 8 -
Para a realização de uma análise, é necessário o preparo de uma solução tampão básica. Estão disponíveis os seguintes reagentes

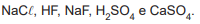
Os reagentes a serem selecionados para o preparo da solução tampão são:
- a) NH4OH e NH4Cl
- b) HCN e NaCN
- c) NaOH e NaCl
- d) HF e NaF
- e) H2SO4 e CaSO4
- #114541
- Banca
- CESGRANRIO
- Matéria
- Química
- Concurso
- UNIRIO
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 9 -
Deseja-se preparar 800 mL de solução aquosa de hidróxido de sódio com pH igual a 12 e a 25 °C.
Assumindo-se completa dissociação do hidróxido de sódio em solução, a massa de base necessária para o preparo da solução, em g, corresponde a

- a) 0,16
- b) 0,24
- c) 0,32
- d) 0,40
- e) 0,48
- #114542
- Banca
- CESGRANRIO
- Matéria
- Química
- Concurso
- UNIRIO
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 10 -
Em um experimento, avaliou-se a seguinte reação química:

As concentrações iniciais de SO2 e O2 foram 0,3 mol/L e 0,2 mol/L, respectivamente. No início da reação, não havia SO3 no reator, mas atingido o equilíbrio, sua concentração foi igual a 0,2 mol/L.
Para esse sistema, a constante de equilíbrio, em termos de concentrações, é igual a
- a) 10
- b) 40
- c) 140
- d) 400
- e) 1400
- #114543
- Banca
- CESGRANRIO
- Matéria
- Química
- Concurso
- UNIRIO
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 11 -
Em um laboratório, estão disponíveis os seguintes sais:
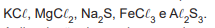
A dissolução de um desses sais em água acarretou a formação de uma solução aquosa com pH ácido.
O sal dissolvido correspondeu a
- a)
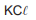
- b)
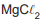
- c)
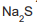
- d)
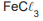
- e)

- #114544
- Banca
- CESGRANRIO
- Matéria
- Química
- Concurso
- UNIRIO
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 12 -
Em um estudo avaliou-se a velocidade da seguinte reação química:
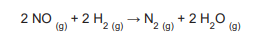
Foram realizados três experimentos distintos, nos quais se variaram as concentrações iniciais dos reagentes, conforme apresentado na Tabela a seguir.
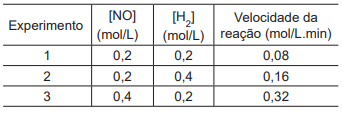
A constante cinética dessa reação química, em L2 mol-2 min-1 , é igual a
- a) 10
- b) 20
- c) 30
- d) 40
- e) 50
- #114545
- Banca
- CESGRANRIO
- Matéria
- Química
- Concurso
- UNIRIO
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 13 -
Uma solução aquosa de cloreto de sódio foi preparada e teve suas temperaturas de ebulição e de congelamento determinadas sob pressão de 1 atm.
Ao se interpretarem os resultados obtidos, conclui-se que a solução salina apresenta:
- a) temperatura de ebulição > 100 °C e temperatura de congelamento < 0 °C
- b) temperatura de ebulição > 100 °C e temperatura de congelamento > 0 °C
- c) temperatura de ebulição < 100 °C e temperatura de congelamento > 0 °C
- d) temperatura de ebulição < 100 °C e temperatura de congelamento < 0 °C
- e) temperatura de ebulição < 100 °C e temperatura de congelamento = 0 °C
- #114546
- Banca
- CESGRANRIO
- Matéria
- Química
- Concurso
- UNIRIO
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 14 -
Em uma prática de laboratório, 1 L de solução aquosa foi obtido ao se misturar 600 mL de solução 0,010 mol/L de cloreto férrico e 400 mL de solução 0,020 mol/L de cloreto de cálcio.
Admitindo-se completa dissociação dos sais, a concentração de íons cloreto na mistura formada, em mol/L, é igual a
- a) 0,022
- b) 0,026
- c) 0,028
- d) 0,030
- e) 0,034
- #114547
- Banca
- CESGRANRIO
- Matéria
- Química
- Concurso
- UNIRIO
- Tipo
- Múltipla escolha
- Comentários
- Seja o primeiro a comentar
(1,0) 15 -
Ácido sulfúrico em excesso foi adicionado a uma amostra de 150 g de alumínio metálico impuro, verificando-se a formação de 10 g de H2 , após a completa reação do alumínio.
Admitindo-se que as impurezas presentes não reagiram com o ácido, o grau de pureza do alumínio é igual a

- a) 50%
- b) 60%
- c) 70%
- d) 80%
- e) 90%

